服务平台拥有丰富的技术服务经验,一流的仪器设备,先进的检测手段和严格的质量控制体系,力求为全球药物研发机构提供优质高效的技术服务
发布日期:2024-07-24
微孔板的选择通常是一个反复的过程,必须平衡各种因素,如自动化兼容性、成本、可用性和性能。这里我们为您总结了微孔板的重要特性,帮助您快速概览可能影响高通量筛选和高内涵成像质量的因素。
微孔板特性
影响高通量筛选和高内涵成像(HCS)质量的微孔板特性包括颜色、孔形、孔容积、孔密度、孔板材质和表面处理[1]。
微孔板颜色
黑色微孔板通常用于荧光应用,而白色微孔板通常支持发光检测,有时还用于增强荧光信号强度。这两种有色板都有助于克服这些技术的关键问题,如背景、自发荧光和孔与孔之间的串扰。
透明- 用于比色实验
白色框架透明底- 用于基于化学发光的底部读数
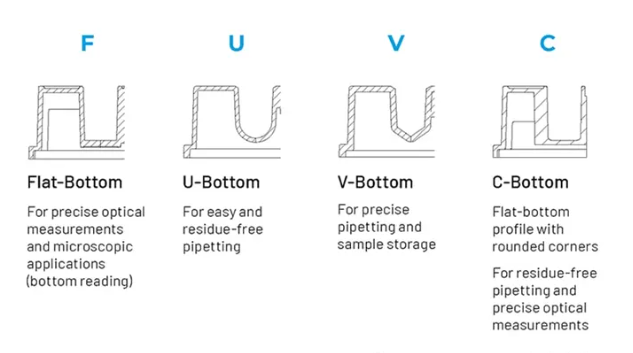
微孔板(底部)材质
在高通量和高内涵筛选以及高分辨率和共聚焦显微镜方面的新应用,增加了对带色壁和透明底的微孔板的需求。Greiner Bio-One 的产品组合包括玻璃底或高质量薄膜底的透明底板。
膜底微孔板(µClear®) 将有色框架与透明底部相结合,是涉及底部读数或显微镜的发光和荧光应用的先决条件。由于优化了薄膜厚度,聚苯乙烯的固有自发荧光被降至最低。
环烯烃薄膜底部的微孔板(SCREENSTAR)是为满足高内涵筛选和高分辨率显微镜的特殊要求而优化设计的。190 µm 的环烯烃薄膜底部确保了即使在高倍显微镜下也能达到最高分辨率。SCREENSTAR微孔板底部凹陷,可充分利用高倍率油浸或水浸物镜,进入所有微孔板周边孔,包括周边和角落位置。
玻璃底微孔板(CELLview)专为高要求、高分辨率的显微应用而设计。它由环烯烃黑色框架和170 微米薄的硼硅玻璃底部组成,可为体外培养物提供优质图像。其几何形状也针对高分辨率显微镜进行了优化,可在较短的工作距离内成像。圆形和锥形孔的设计减少了半月板效应,以确保细胞分布均匀和成像效果稳定。
透明solid底 - 用于顶部和底部读数(波长>400 nm 时仅底部读数)。
黑色或白色solid底 - 用于顶部读数
聚苯乙烯薄膜底(µClear®) - 用于 340 nm以下的显微镜和光谱测量(340-400 nm)
环烯烃薄膜底(UV-Star®) - 用于紫外光谱(230-340 nm)
环烯烃薄膜底(SCREENSTAR)- 用于高倍显微镜观察
玻璃底(CELLview)- 用于高倍显微镜观察
表面处理

在孔表面,样品和微孔板之间会发生相互作用。因此,表面特性对孔板的功能起着重要作用。可以通过物理、化学或包被等多种方法改变表面特性,以满足各种需求。
未经处理表面 -用于均相检测
无结合表面 - 用于敏感的均相检测
中等结合力表面- 用于免疫测定
高结合力表面 -用于免疫测定
链霉亲和素包被表面- 用于免疫测定
组织培养(TC)处理--用于一般贴壁细胞培养
悬浮 - 用于非贴壁细胞培养
加强 TC - 用于培养苛刻的细胞系
蛋白质包被(聚(D±L)-赖氨酸(PDL、PLL)、ECM包被--用于满足细胞生长和贴壁的特定需要
细胞排斥表面--用于细胞球和类器官的形成
用于生物检测的微孔板
用于生物检测的微孔板应符合以下标准:[2]
在多种温度和湿度条件下的尺寸稳定性
平整度
与检测试剂的化学和生物兼容性
化学或生物吸附性低
自发荧光少
支持细胞存活、贴壁和生长
支持相关光学检测模式
无溶剂、金属或化学品浸出
HCS 成像仪器光学元件和微孔板规格
HCS 成像设备的光学元件必须与微孔板的规格相匹配。实验需要考虑微孔板规格的各个方面以及物镜的以下关键特性:
放大倍数
数值孔径
工作距离
景深
最小 Z 平面间距
其他考虑因素
光学各向同性--这对于成像检测和涉及偏振光的检测非常重要,因为各向异性的材料会产生光干扰
参考文献
[1] Auld DS Ph.D., Coassin PA B.S., Coussens NP Ph.D., et al. Microplate Selection and Recommended Practices in High-throughput Screening and Quantitative Biology. In: Markossian S, Grossman A, Brimacombe K, et al., eds. Assay Guidance Manual. Bethesda (MD): Eli Lilly & Company and the National Center for Advancing Translational Sciences; June 1, 2020. https://pubmed.ncbi.nlm.nih.gov/32520474/
[2] Auld DS Ph.D., Coassin PA B.S., Coussens NP Ph.D., et al. Microplate Selection and Recommended Practices in High-throughput Screening and Quantitative Biology. In: Markossian S, Grossman A, Brimacombe K, et al., eds. Assay Guidance Manual. Bethesda (MD): Eli Lilly & Company and the National Center for Advancing Translational Sciences; June 1, 2020. https://pubmed.ncbi.nlm.nih.gov/32520474/
